從先進技術轉化癌症治療的未來正在迅速接近。使用治療性核酸的創新策略,指導細胞與癌症等疾病作鬥爭的必需分子正在鋪路。挑戰是這些分子在細胞中的分佈,類似於通過難以穿透的壁傳遞的秘密信息。這不僅是猜測,而且是最後一個進步的本質。小型專門的載體,稱為納米金屬有機框架(納米群),旨在將這些必需分子直接運輸到癌細胞的心臟,從而導致長期以來一直是障礙的自然防禦。除了消息分佈之外,這種方法可確保達到正確的接收者,集中癌症治療,而沒有癌症,而沒有傳統療法的副作用。這一重大進展將改變與癌症的鬥爭,這標誌著基因治療的先驅時刻。
在一項由巴黎 – 薩克萊大學的首席作者Ruxandra Gref領導的開創性研究中,以及北卡羅來納大學夏洛特大學的Kirill Afrony博士,與他們的團隊一起編寫Juan Casas-Solvas博士和Almería的Antonio Vargas-Bengel教授Almería的Almería,Almería的AlmeríaPatriarcheDr.夏洛特北卡羅來納大學的摩根·錢德勒(Morgan Chandler)博士和巴黎 – 薩克萊大學的Xue li博士在《國際藥品公報:X》中發現了一種新的癌症治療方法:X,顯示了納米膽道 – 有機金屬框架(Nanomofs)在基因治療中的廣泛潛力。最初的研究表明,納米群如何直接將核糖治療酸給癌細胞,從而在與這種廣泛的疾病作鬥爭中打開新的門。
訪問使用納米型工程將核糖治療酸包裝到癌細胞中。這涉及基因療法中的重要挑戰:核酸的攝入源是通過細胞膜負電荷的。這些經過精心設計的納米植物不僅克服了這一障礙,而且還可以使特定癌細胞的靶標,從而提高了治療的有效性。
Afonin博士闡明了他們的發現:“我們已經成功地使用了由Ruxandra Gref團隊開發的納米型,以在癌細胞中提供核糖治療酸,這證明了MDA-MOM-231乳腺癌細胞中報告基因表達的顯著降低。”這一進展為更有效的癌症治療打開了大門,允許將遺傳物質的預期分佈直接傳播到腫瘤細胞上。
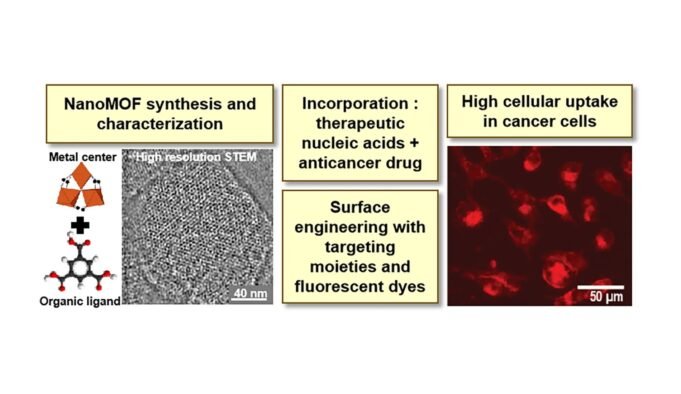
研究小組使用複雜的方法來開發和評估納米群,從使用微波輔助的過程使用氯化鐵和苯岑-1,3,5-三核酸的合成開始。隨後的修飾會增加納米類的表面,以更有效地旨在癌細胞,尤其是通過引入P-CD-M來增加細胞親和力。核酸為納米群的整合製備是一個細緻的步驟,它涉及大量優化方案,以實現核酸兌核的最佳保護並保持其完整性,從而確保它們在分佈過程中的有效性。通過動態光分佈(DLS)和跟踪納米顆粒(NTA)的分析來表徵納米群的表徵,證實了它們的適當大小,穩定性和成功的核酸電荷,證明了它們在現實世界應用中的潛力。
進行了幾項測試以驗證納米類的有效性,包括研究從細胞中獲取納米群的研究以及它們沉默的特定基因的能力。這些測試表明,納米群有效進入癌細胞並給出其核酸碳的能力,從而導致所需的治療作用。
這項研究的含義很重要,為癌症治療提供了新的有希望的途徑。通過允許將治療性核酸準確地分佈到腫瘤細胞中,納米群具有提高基因治療的準確性和效率,最大程度地減少副作用並改善患者的結果。 Afonin博士強調:“不同的治療劑的組合導致了更重要的治療作用”,這強調了在治療中使用納米群的潛力,以取得更好的結果。
這項創新的工作置於探索和進一步發展基於納米的療法的基礎。需要對結構功能的更全面的研究來擴展到當前平台,以顯示這一激動人心的研究領域的未來方向。成功地應用納米群在基因療法中可以改變癌症治療,為全球數百萬患者提供新的希望。總之,對Gref博士和Aftoni博士的研究發現,納米群為癌症治療提供了新的途徑,有效地提供了靶細胞中的核酸治療,並提高了治療效率。他們的研究證實了納米類的保護和分配技巧,強調了創新,入侵療法的潛力。
日記
X. Li等人,“用於癌細胞中核酸分佈的納米金屬有機框架”,《國際藥物雜誌:x 5(2023)100161。 doi: https://doi.org/10.1016/j.ijpx.2023.100161。