正常細胞會變老,並在達到最大預期壽命時死亡。在這些端粒細胞中,由於抑制了人端粒酶(HTTT)的逆轉錄酶,因此無法合成染色體的末端,這導致端粒縮短。
儘管該連接仍不清楚,但許多研究表明,HTTT的重新激活導致端粒的維持,這可能導致癌症。同時,結果表明,一對端粒結合蛋白與G-Kuadruplexes相互作用。
由於HTERT啟動子包含了G-四鏈體的形成眾多序列,因此在最近的一項研究中,科學家研究了端粒 – 反應器因子2(TRF2)是否與啟動子相關,並且這是否對HTERT調節有影響。 Professor Shantanu Chowrsh, Shalu Sharma, Ananda Kishore Mukherjee, Shuvra Shekhar Roy, Sulochana Bagri, Dr. Meenakshi Verma, Antaraa Sengupta, Manish Kumar in the Csir-Intensive Genomics and Integration Biology in Collabim with Deo Prakash Pandey Silje Lier, and Gaute Nesse atmo atmo atmo them Oslo them奧斯陸。發現了由HTERT調節因子介導的端粒機制,建立了端粒和端粒酶之間的分子鍵,這對於腫瘤轉化,衰老和再生療法至關重要,該療法發表在 細胞比率。
科學家通過脊椎動物確定了行啟動子的序列,用於G Quadruplex。他們還進行了CHIP分析(染色質免疫沉澱)並進行了分析。同時,由於CRF2是與端粒相關的真正蛋白質,因此將端粒PCR用作CRF2芯片的陽性檢查。後來,他們進行了串行實驗,包括蛋白質免疫沉澱,免疫熒光顯微鏡,以計算TF2和HTERT信號的強度,免疫 – 流動細胞儀,實時PCR,印跡分析,ELISA,ELISA和其他分子測試。
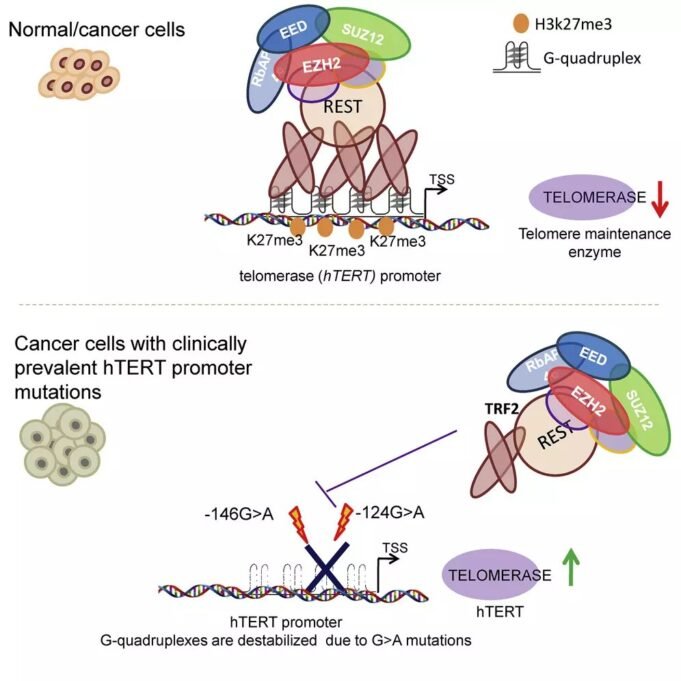
Chowrsh教授及其同事表明,CRF2直接與HTERT啟動子相互作用,並控制癌症和正常細胞中的HTERT和端粒酶活性。他們還發現,TF2的MYB和主田都需要調節HTERT轉錄。 TRF2調節HTERT啟動子中染色質的表觀遺傳狀態;由HTERT啟動子中Polycomb抑製劑複合物(PRC2)的TF2引起的募集。
該小組透露,與HTERT啟動子的CRF2關聯不是端粒依賴的,而是取決於G Quadruplex。此外,在具有HTTT啟動子突變的癌症中,CRF2損失的職業以及通過配體穩定G-Kadruplex,將TF2連接重置,並抑制活化的端粒酶。
他們的發現將有助於更多地了解有關維持端粒和端粒酶調節的衰老,癌症,細胞衰老和DNA損傷反應過程。主要作者教授Chowhraly說:“癌症中的雜貨末期特別重要。儘管將需要進一步的工作來證明這一點,根據我們在此處的發現,通過TRF2創建了端粒 – telomer-telomerase crosstalk(通過TROMERIC(端粒)(促進性HTERT中的非tutelomeric bongions thertemeric bongionals httert)可以鍵入Telomeres的鍵。
他還補充說:“相對改善的端粒酶水平和長端粒水平對於多能幹細胞的維持/存活至關重要。”因此,與端粒相關的TF2介導的HTERT調整在Plurpottia中可能很重要。
這項研究首次表明,使用小分子配體在多形膠質母細胞瘤和其他癌症中由HTET TF2引起的重新分配提供了可能的治療選擇。小分子被調整以連接和穩定G-四鏈體。 “這些結果為開髮用於多形膠質母細胞瘤的治療干預的G四鏈體分子提供了有趣的機會。” Chowhry教授說。此外,使HTERT處於正常細胞中抑制狀態的機制以及其解析導致HTERT對癌細胞重新激活的機制。
Chowhraly教授說:“總之,這些結果表明端粒與端粒酶之間的分子聯繫對於推進對細胞智能功能的理解,包括腫瘤轉化,衰老和多重性/分化至關重要。”

日記參考:
Sharma S,Mukherjee AK,Roy SS,Bagri S,Lier S,Verma M,Sengupta A,Kumar M,Nesse G,Nesse G,Pandey DP,Chowhrahy S.人端粒酶直接由非TELF2-G-Quadruplex互動直接調節。眾議員Cell 2021 5月18日; 35(7):109154。 doi:10.1016/j.celrep.2021.109154。 PMID:34010660。
關於

Sharma Sharma博士博士
完成我的微生物學碩士學位後,2014年Shalu Sharma博士在CSIR-IGIB上加入Shantanu Chowhraly博士,獲得博士學位。 SC實驗室研究癌症的重點是Telomera的生物學。它首先探索端粒對細胞衰老和廣泛基因組轉錄組學的調節作用。逐漸地,它對理解人端粒酶的調節產生了興趣,在癌症中激活了超級癌症。研究小組的最新發現揭示了端粒如何向端粒酶調整髮出信號。作為端粒酶啟動子中的臨床突變會導致端粒酶過度激活。基於此,團隊發現了將DNA連接用於治療干預的小分子的潛力。

Ananda K Mukherjee博士,,,, 醫生
Ananda K Mukherjee博士於2014年在IGIB的Shantanu Chowrsh博士實驗室中加入研究生,在那裡他被介紹給Telomere Biology和Telomere,將蛋白質-TRF2連接起來。該小組對TF2的非通道轉錄效應取決於端粒的長度進行了有趣的觀察。然後,他們指出,CRF2直接抑制端粒酶,同時使用基因啟動子中的G-Kadruplexes維持抑制的組蛋白。他們進一步發現,破壞膠質母細胞瘤突變的特定G-四鏈體導致該調節的喪失。他目前正在試圖弄清腫瘤細胞端粒長度的異質性如何影響對癌症的免疫反應。

Shantanu Chowrsh教授博士
Shantanu Chowhry目前是德里CSIR基因組學和綜合生物學的教授。它的研究興趣包括理解稱為G四鏈體的非二值DNA結構的功能。特別是,在癌症中的端粒酶控制和端粒功能中。 2002年,他搬到了目前的職位,在那裡他開始了實驗室。 2012年,Shantanu獲得了生物科學(印度最負盛名的科學價格)的Shanti Swarup Batnagar獎。他是DBT / Wellcome Trust India Alliance的老成員,並且是生物化學報紙編輯委員會成員。
主要圖像來源:Chowredy等人 https://dii.org/10.1016/j.celrep.2021.109154